Manual del Curso de Patron de Yate de Vela y Motor
![]() San Isidro, Argentina
San Isidro, Argentina
![]() CVPB - Jorge Messano
CVPB - Jorge Messano
![]() 31-Mar-2026
31-Mar-2026
![]() 12 minutos
12 minutos
Capítulo 01: Meteorología
Parámetros Atmosféricos: La Humedad Relativa
Introducción
La humedad relativa, o simplemente la humedad, es un parámetro clave para entender el comportamiento del aire y su capacidad para contener vapor de agua. Aunque solemos pensar en la humedad como “agua en el ambiente”, en realidad se trata de la proporción entre la cantidad de vapor que el aire contiene en un momento dado y la cantidad máxima que podría contener a esa misma temperatura. Esta relación es importante porque la temperatura determina el límite de saturación del aire: cuanto más cálido está, más vapor puede retener; cuanto más frío, menos.
Por este motivo, la humedad relativa desempeña un papel central en numerosos procesos atmosféricos —formación de nubes, nieblas, precipitaciones, y sensación térmica— y, junto con la temperatura y la presión, completa el trío de variables esenciales que gobiernan la dinámica del tiempo meteorológico.
Definiciones
La humedad, en el contexto de los parámetros atmosféricos, es la cantidad de vapor de agua contenida en el aire en un momento dado.
Dos factores se consideran para evaluar la humedad del aire:
Humedad Relativa
Es la relación entre la cantidad de vapor de agua que contiene una masa de aire a una temperatura dada y la cantidad máxima que podría contener cuando está saturada a esa misma temperatura.
La saturación ocurre cuando el aire ya no puede seguir incorporando vapor de agua y comienza a devolverlo en forma líquida —como pequeñas gotas de rocío—. Ese estado corresponde al 100% de humedad relativa.
Se denomina “relativa” porque depende directamente de la temperatura y la presión del aire: el aire cálido puede retener más vapor antes de saturarse, mientras que el aire frío alcanza la saturación con menor cantidad de vapor.
Punto de Rocío
Es la temperatura a la cual una masa de aire debe enfriarse para alcanzar su punto de saturación. Una vez alcanzada esa temperatura, el aire deja de admitir más vapor y comienza a condensarlo, devolviéndolo al estado líquido —como pequeñas gotas de agua—.
El punto de rocío se hace visible cuando esa humedad condensada se deposita en forma de gotas —rocío, neblina en superficies frías, empañamiento de vidrios, por ejemplo— al entrar en contacto con objetos o superficies más frías que el aire circundante.

La Ley de Dalton, o Ley de las Presiones Parciales, que establece que la presión total de una mezcla de gases es la suma de las presiones parciales ejercidas por cada uno de sus componentes —y el aire es justamente una mezcla— permite explicar el comportamiento del vapor de agua en la atmósfera.
Así entonces, si la temperatura del aire permanece constante y aumenta la cantidad de vapor de agua, la humedad relativa también aumenta. Es decir, al incorporar más vapor a un volumen de aire cuya temperatura no varía, el vapor de agua ocupa una mayor fracción de la presión total, acercándose de a poco al punto de saturación.
Por otro lado, si la temperatura del aire aumenta mientras la cantidad de vapor de agua permanece constante, la humedad relativa disminuye. Esto ocurre porque un aire más cálido puede contener mucha más cantidad de vapor antes de saturarse: la presión de vapor de saturación aumenta con la temperatura, de modo que el aire se “aleja” del punto de rocío.
Finalmente, si la cantidad de vapor de agua permanece constante y la temperatura del aire desciende, la humedad relativa aumenta. Al enfriarse, disminuye la presión de vapor de saturación: el aire pierde capacidad para retener vapor de agua, por lo que se acerca rápidamente al punto de saturación y puede alcanzarlo, dando lugar a la condensación.
John Dalton fue un químico y físico británico —vivió entre 1776 y 1844— al que debemos la primera formulación moderna de la teoría atómica, importantes aportes al estudio de los gases y, de manera indirecta, el nombre del daltonismo.
Cuenta la historia que, cuando tenía 26 años, le regaló a su madre un par de medias azules. Ella, sorprendida, le preguntó por qué le obsequiaba medias moradas, un color que no consideraba apropiado para una mujer cuáquera —era un movimiento cristiano que promovía la sencillez y el vestir sobrio, evitando los colores llamativos—. Su hermano, presente en la escena, intervino asegurando que las medias eran efectivamente moradas.
La discrepancia llamó tanto la atención de John y su hermano que se pusieron a estudiar el tema, y dos años más tarde publicaron un artículo científico describiendo el trastorno visual que les afectaba, y que más adelante sería conocido como daltonismo.

Unidades de Medida e Instrumentos de Medición
La humedad relativa se mide con el higrómetro —también se utilizan psicrómetros, que miden la humedad a partir de la diferencia de temperaturas— y el higrógrafo se utiliza para registrar la humedad relativa en el tiempo.
Dado que la humedad relativa depende de la temperatura, generalmente los higrómetros e higrógrafos se asocian a termómetros y termógrafos.
El punto de rocío se obtiene en general con un psicrómetro.
Los psicrómetros están compuestos por dos termómetros, donde uno toma la temperatura de un paño húmedo que envuelve el bulbo de mercurio y el otro la del aire. La diferencia de temperaturas entre ambos termómetros indica la diferencia entre la temperatura actual y el punto de rocío.

Ciclo Hidrológico
El agua interactúa constantemente con la atmósfera a través del ciclo hidrológico —también llamado ciclo del agua—, un proceso continuo mediante el cual el agua cambia de estado físico y se desplaza entre océanos y masas de agua, continentes y atmósfera.
Evaporación
El agua de los océanos, mares, lagos, ríos y superficies húmedas pasa del estado líquido al gaseoso, incorporándose a la atmósfera como vapor de agua. Este proceso está impulsado por la radiación solar y por la temperatura del aire.
Condensación
A medida que asciende, el vapor de agua alcanza capas más frías de la atmósfera. Allí se condensa, primero formando diminutas gotas de agua líquida que originan las nubes. Si continúa elevándose y supera la cota del punto de congelación, estas gotas se transforman en cristales de hielo, dando lugar a nubes formadas por partículas heladas.
Precipitación
Cuando las gotas o cristales de hielo dentro de una nube crecen lo suficiente como para vencer la resistencia del aire, precipitan. Lo hacen en forma de llovizna, lluvia, nieve o granizo, dependiendo de las condiciones térmicas de la columna atmosférica. El agua precipitada vuelve a ríos, arroyos, lagos y napas subterráneas, alimentando nuevamente el ciclo.
El proceso de cambio de estados del agua requiere del intercambio de energía entre las moléculas de H2O y las de los otros gases que componen el aire, o con las superficies con las que entra en contacto. Esto sucede debido al mismo principio de equilibrio energético que se aplica a la circulación general de la atmósfera.
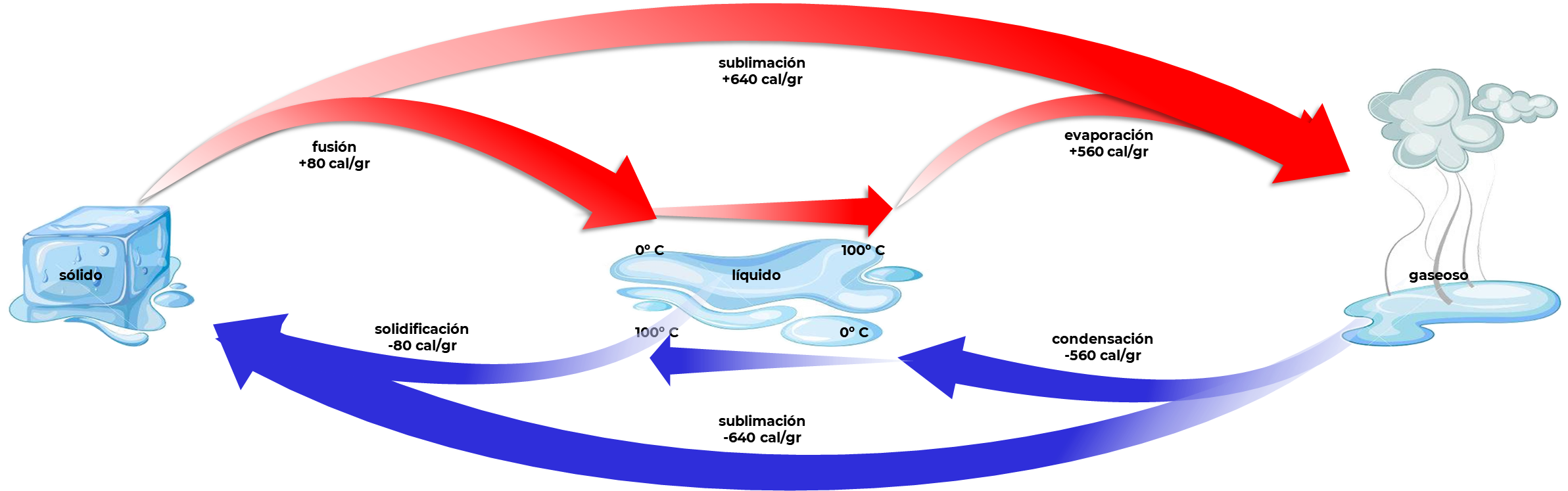
Fusión
Es el proceso de pasaje del estado sólido al líquido.
Esto ocurre, por ejemplo, cuando se derrite el hielo de las cimas de las montañas y de los glaciares, o cuando el granizo o la nieve se convierten en agua al entrar en contacto con la superficie más caliente del suelo.
En este proceso, las moléculas de agua que forman el hielo deben absorber energía —80 calorías por gramo— a fin de poder calentarse. Esa energía es tomada de la radiación solar y por intercambio directo con las otras moléculas que componen el aire o la superficie donde ese hielo está apoyado, las cuales, por consecuencia, se enfrían.
Este intercambio de energía se ve muy bien cuando se le agrega, por ejemplo, cubitos de hielo a una bebida para enfriarla.
El resultado será que las moléculas de H2O del hielo tomaron energía de las moléculas de la bebida, calentándose, y pasando así al estado líquido. Y en el mismo proceso, la bebida perdió calor, porque se lo entregó al agua del hielo, enfriándose.
Evaporación
Es el pasaje del estado líquido al gaseoso.
Ocurre cuando el agua de los mares, lagos y ríos se evapora producto del calor intercambiado con la atmósfera y aportado por la radiación solar.
La cantidad de energía necesaria para lograr la evaporación del agua es de alrededor de 560 calorías por gramo. Las moléculas que componen el aire se enfriarán durante este proceso.
Un ejemplo más cercano a nosotros del proceso de evaporación es el que se ve cuando uno toma una ducha de agua caliente, y el agua se hace visible como vapor, formando una especie de niebla blanquecina que se eleva.
Las moléculas de H2O del aire son las que, al entrar en contacto con el agua sobrecalentada de la ducha, adquieren de ella la energía suficiente para pasar al estado gaseoso.
La cantidad de vapor que se forme dependerá del porcentaje de humedad relativa, cuanto mayor sea —es decir, cuanto más saturado de humedad esté el aire— más vapor se formará, mientras que en días o ambientes con bajo porcentaje de humedad relativa, menor será el vapor que se forme.
Esto a su vez sirve para explicar que la evaporación del agua es un proceso que ocurre inclusive a temperatura ambiente, sin necesidad de que llegue a la del punto de ebullición.
La evaporación sucede a medida que las moléculas de H2O en estado líquido, adquieren suficiente energía del medio como para pasar al estado gaseoso.
Eso pasa, por ejemplo, cuando se tiende la ropa mojada al Sol, para que se seque.
Condensación
Es el proceso inverso a la evaporación.
El vapor de agua se enfría volviendo al estado líquido. Sucede, por ejemplo, durante la formación de la lluvia, cuando las moléculas de vapor de agua entran en contacto con corrientes de aire más frías con las cuales intercambian energía, agrupándose y regresando al suelo al estado líquido en forma de gotas de lluvia o llovizna.
Este proceso libera unas 560 calorías por gramo, que pasan del vapor de agua al aire o a los materiales con los que entra en contacto.
He aquí la explicación de por qué se humedece el techo del baño al tomar la ducha.
El vapor de agua se enfría al tomar contacto con las superficies más frías —la del techo del baño en este caso— entregando energía y regresando al estado líquido.
Solidificación
Es el proceso inverso a la fusión.
El agua en estado líquido pasa a estado sólido, convirtiéndose en hielo.
Este proceso sucede, por ejemplo, dentro de las nubes de tormenta —los Cumulonimbus— cuando el vapor de agua se eleva desde la parte baja de la nube, enfriándose a medida que asciende, pasando primero al estado líquido, y luego al sólido formando granizo al llegar al tope nuboso en el cual las temperaturas están por debajo de los 0º C.
Este proceso libera 80 calorías por gramo que pasan del agua a la atmosfera.
Sublimación
Es el proceso de paso del agua del estado sólido al gaseoso y viceversa, sin pasar por el estado líquido.
Al primer caso se lo denomina sublimación, y al segundo se lo identifica también como sublimación regresiva.
El caso más conocido de sublimación es lo que ocurre con el hielo seco, que se evapora sin formar líquidos. Y la sublimación regresiva sucede cuando, por ejemplo, se forma nieve en las paredes del congelador al abrirlo.
En la próxima nota entraremos en la explicación de cómo y porque ocurre el viento.
Fuentes
Este texto forma parte del Manual de Instrucción del Curso de Patrón de Yate de Vela y Motor de la Escuela de Náutica del Club de Veleros Piedrabuena.
ISBN 978-987-88-1913-6
Reproducido con autorización del autor.

 inicio
inicio
 escuela
escuela
 nota anterior
nota anterior
 nota siguiente
nota siguiente